Chưa có sản phẩm trong giỏ hàng.
Thuốc Ritonir là thuốc gì, giá bao nhiêu mua ở đâu điều trị Covid
- Đăng tải: Phan Tuấn
Liên hệ để biết giá !
Thuốc Ritonir được điều trị để điều trị Covid-19 ở người lớn và những người có nguy cơ cao tiến triển thành Covid-19 nặng.
Thuốc Ritonir là thuốc kháng virus COVID-19 sử dụng đường uống. Thành phần thuốc bao gồm Nirmatrelvir (chất ức chế protein của SARS-CoV-2) để ngăn ngừa virus nhân lên và hoạt chất Ritonavir làm chậm đi quá trình phân hủy của Nirmatrelvir giúp cho thuốc tồn tại trong cơ thể được lâu hơn và tồn tại ở nồng độ cao hơn.
Trong bài viết này, nhà thuốc hapu xin gửi đến quý khách hàng thông tin chi tiết về Thuốc Ritonir. Nếu quí khách hàng còn bất kì thắc mắc nào vui lòng gọi đến sdt hotline 092328303 để được tư vấn hỗ trợ và giải đáp
Nhathuochapu.vn Chuyên tư vấn, mua bán các loại các loại thuốc kê đơn (Ung thư, viêm gan B, C, thuốc điều trị vô sinh hiếm muộn, kháng sinh…) và các loại thuốc hiếm khó tìm.
Danh mục: Sản phẩm phòng chống Covid
Từ khóa: Covid, Điều trị Covid, Mua thuốc Paxlovid ở đâu, Mua thuốc Paxlovid ở đâu Hà Nội, Mua Thuốc Ritonir ở đâu Hà Nội, Mua Thuốc Ritonir ở đâu HCM, Thuốc điều trị covid, Thuốc Molravir, Thuốc Paxlovid, Thuốc Primovir, Thuốc Ritonir, Thuốc Ritonir giá bao nhiêu, Thuốc Ritonir là thuốc gì, Thuốc Ritonir mua ở đâu
Thuốc Ritonir được điều trị để điều trị Covid-19 ở người lớn và những người có nguy cơ cao tiến triển thành Covid-19 nặng.
Thuốc Ritonir là thuốc kháng virus COVID-19 sử dụng đường uống. Thành phần thuốc bao gồm Nirmatrelvir (chất ức chế protein của SARS-CoV-2) để ngăn ngừa virus nhân lên và hoạt chất Ritonavir làm chậm đi quá trình phân hủy của Nirmatrelvir giúp cho thuốc tồn tại trong cơ thể được lâu hơn và tồn tại ở nồng độ cao hơn.
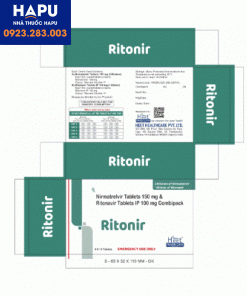
Thông tin cơ bản về thuốc Ritonir
-Thành phần: Nirmatrelvir hàm lượng 150mg
Ritonavir hàm lượng 100mg
-Dạng bào chế: Viên nén
-Quy cách đóng gói: Hộp gồm 3 vỉ x 10 viên

Chỉ định điều trị thuốc Ritonir
Thuốc Ritonir được chỉ định dùng cho đối tượng bệnh nhân:
Thuốc Ritonir được chỉ định để điều trị COVID-19 ở người lớn không cần bổ sung oxy và những người có nguy cơ cao mắc COVID-19 nặng
Liều lượng và cách dùng thuốc Ritonir
Thuốc Ritonir là một thuốc gồm viên nén nirmatrelvir được đóng gói cùng với một viên ritonavir.
Thành phần Nirmatrelvir phải được sử dụng kết hợp đồng thời với thành phần ritonavir. Việc không kết hợp đúng cách nirmatrelvir với ritonavir sẽ dẫn đến nồng độ nirmatrelvir trong huyết tương sẽ không đủ để đạt được hiệu quả điều trị mong muốn.
Liều lượng khuyến cáo là 300 mg nirmatrelvir (hai viên 150 mg) với 100 mg ritonavir (một viên 100 mg), tất cả được uống cùng nhau hai lần mỗi ngày trong 5 ngày. Thuốc Ritonir nên được dùng càng sớm càng tốt sau khi có kết quả xét nghiệm vi rút SARS-CoV-2 trực tiếp dương tính và trong vòng 5 ngày kể từ khi xuất hiện các triệu chứng.
Thuốc Ritonir có thể uống cùng hoặc không cùng thức ăn. Viên nén nên được nuốt cả viên và không được nhai, bẻ hoặc nghiền nát.
Trong trường hợp bệnh nhân quên liều thì nên uống ngay sau khi nhớ ra trong vòng 8 giờ kể từ thời gian dự kiến, và lịch trình dùng thuốc bình thường nên được tiếp tục. Nếu hơn 8 giờ trôi qua, không dùng liều đã quên và tiếp tục điều trị theo lịch dùng thuốc bình thường.
Nếu bệnh nhân cần nhập viện do nhiễm COVID-19 nghiêm trọng hoặc nguy kịch sau khi bắt đầu điều trị bằng Thuốc Ritonir thì bệnh nhân đó phải hoàn thành toàn bộ liệu trình điều trị kéo dài 5 ngày theo quyết định của nhà cung cấp dịch vụ chăm sóc. sức khoẻ của anh ấy.
Đối tượng bệnh nhân đặc biệt
Trẻ em
Tính an toàn và hiệu quả của Thuốc Ritonir ở bệnh nhi dưới 18 tuổi chưa được thiết lập.
Người cao tuổi
Hiện không khuyến cáo điều chỉnh liều cho bệnh nhân cao tuổi.
Suy thận
Không cần điều chỉnh liều ở đối tượng bệnh nhân bị suy thận nhẹ.
Ở những bệnh nhân suy thận vừa phải, nên giảm liều Thuốc Ritonir xuống còn nirmatrelvir/ritonavir 150 mg/100 mg (1 viên mỗi loại) hai lần mỗi ngày trong 5 ngày. Các viên nirmatrelvir còn lại nên được xử lý theo yêu cầu của địa phương
Thuốc Ritonir không được khuyến cáo ở bệnh nhân suy thận nặng hoặc suy thận vì chưa xác định được liều thích hợp
Suy gan
Không cần điều chỉnh liều Thuốc Ritonir đối với bệnh nhân suy gan nhẹ (Child-Pugh Loại A) hoặc trung bình (Child-Pugh Loại B).
Không có dữ liệu dược động học hoặc an toàn liên quan đến việc sử dụng nirmatrelvir hoặc ritonavir ở những đối tượng bị suy gan nặng (Child-Pugh Class C), do đó, Thuốc Ritonir bị chống chỉ định ở những bệnh nhân bị suy gan. nặng.
Điều trị đồng thời với chế độ điều trị có chứa ritonavir hoặc cobicistat
Không cần điều chỉnh liều lượng; Liều Thuốc Ritonirlà 300 mg/100 mg hai lần mỗi ngày trong 5 ngày.
Bệnh nhân được chẩn đoán nhiễm vi rút gây suy giảm miễn dịch ở người (HIV) hoặc vi rút viêm gan C (HCV) đang điều trị bằng phác đồ có chứa ritonavir hoặc cobicistat nên tiếp tục điều trị theo chỉ định.
Chống chỉ định thuốc Ritonir
Thuốc Ritonir chống chỉ định ở những đối tượng bệnh nhân sau:
– Tiền sử quá mẫn đáng kể về mặt lâm sàng với các thành phần hoạt chất (nirmatrelvir/ritonavir) hoặc với bất kỳ tá dược nào
– Suy gan nặng.
– Bị suy thận nặng.
Thuốc Ritonir cũng chống chỉ định với các sản phẩm thuốc phụ thuộc nhiều vào CYP3A để thanh thải và nồng độ trong huyết tương tăng cao có liên quan đến các phản ứng nghiêm trọng và/hoặc đe dọa tính mạng. Thuốc Ritonir cũng bị chống chỉ định với các sản phẩm thuốc gây cảm ứng mạnh CYP3A khi nồng độ nirmatrelvir/ritonavir trong huyết tương giảm rõ rệt có thể liên quan đến khả năng mất đáp ứng và kháng virus.
Sử dụng thận trọng
Nguy cơ gây ra một số phản ứng có hại nghiêm trọng khi thuốc Ritonir tương tác với các sản phẩm thuốc khác
Bắt đầu dùng Ritonir, một chất ức chế CYP3A, ở những bệnh nhân đang dùng các sản phẩm thuốc được chuyển hóa bởi CYP3A hoặc bắt đầu dùng các sản phẩm thuốc được chuyển hóa bởi CYP3A ở những bệnh nhân đã dùng huốc Ritonir, có thể làm tăng nồng độ trong huyết tương của một số các sản phẩm thuốc được chuyển hóa bởi CYP3A.
Việc bắt đầu dùng các sản phẩm thuốc ức chế hoặc cảm ứng CYP3A có thể làm tăng hoặc giảm nồng độ Ritonir tương ứng.
Những tương tác thuốc này có thể dẫn đến:
Các phản ứng có hại đáng kể về mặt lâm sàng có khả năng dẫn đến các biến cố nghiêm trọng, đe dọa đến tính mạng hoặc tử vong do tiếp xúc nhiều hơn với các sản phẩm thuốc dùng đồng thời.
Các phản ứng có hại đáng kể về mặt lâm sàng do phơi nhiễm Ritonir nhiều hơn.
Ritonir mất tác dụng điều trị và có thể phát triển khả năng kháng thuốc đối với vi rút.
Các tương tác tiềm tàng nên được xem xét với các sản phẩm thuốc khác trước và trong khi điều trị với huốc Ritonir;
Các sản phẩm thuốc đồng thời nên được xem xét trong quá trình điều trị với huốc Ritonirvà bệnh nhân nên được theo dõi các phản ứng bất lợi liên quan đến các sản phẩm thuốc đồng thời. Nguy cơ tương tác với các thuốc dùng đồng thời trong quá trình điều trị 5 ngày với huốc Ritonir nên được cân nhắc với nguy cơ không dùng thuốc Ritonir
Nhiễm độc gan
Tăng men gan, viêm gan lâm sàng và vàng da đã xảy ra ở những bệnh nhân dùng ritonavir. Do đó, nên thận trọng khi dùng Thuốc Ritonir cho bệnh nhân mắc bệnh gan từ trước, bất thường men gan hoặc viêm gan.
Kháng HIV
Vì nirmatrelvir được dùng cùng với ritonavir nên có thể có nguy cơ HIV-1 phát triển khả năng kháng thuốc ức chế protease HIV ở những đối tượng bệnh nhân bị nhiễm HIV-1 không được kiểm soát hoặc không được chẩn đoán.
Tá dược
Viên nén Nirmatrelvir có chứa đường sữa. Bệnh nhân có vấn đề di truyền hiếm gặp về không dung nạp galactose, thiếu hụt lactase toàn phần hoặc kém hấp thu glucose-galactose không nên dùng thuốc này.
Mỗi viên Nirmatrelvir và ritonavir chứa ít hơn 1 mmol natri (23 mg) mỗi liều, nghĩa là về cơ bản nó ‘không có natri’..
Tương tác Thuốc Ritonir với các sản phẩm thuốc khác và các dạng tương tác khác
Thuốc Ritonir (nirmatrelvir/ritonavir) là chất ức chế CYP3A và có thể làm tăng nồng độ trong huyết tương của các sản phẩm thuốc được chuyển hóa chủ yếu bởi CYP3A. Các sản phẩm thuốc được chuyển hóa mạnh bởi CYP3A và có chuyển hóa bước đầu cao dường như dễ bị tăng phơi nhiễm nhất khi dùng đồng thời với nirmatrelvir/ritonavir.
Do đó, chống chỉ định sử dụng đồng thời nirmatrelvir/ritonavir với các sản phẩm thuốc phụ thuộc nhiều vào CYP3A để thanh thải và tăng nồng độ trong huyết tương liên quan đến các biến cố nghiêm trọng và/hoặc đe dọa tính mạng
Các nghiên cứu in vitro cho thấy nirmatrelvir có thể cảm ứng CYP3A4, CYP2B6, CYP2C8 và CYP2C. Dựa trên dữ liệu in vitro, nirmatrelvir có khả năng ức chế BCRP, MATE2K, OAT1, OAT3, OATP1B3 và OCT2 thấp. Nirmatrelvir có khả năng ức chế MDR1, MATE1, OCT1 và OATP1B1 ở nồng độ phù hợp về mặt lâm sàng.
Thành phần hoạt chất Ritonavir chứa trong thuốc Ritonircó ái lực cao với một số đồng dạng cytochrom P450 (CYP) và có thể ức chế quá trình oxy hóa theo thứ tự xếp hạng sau: CYP3A4 > CYP2D6.
Ritonavir chứa trong thuốc Ritonir cũng có ái lực cao với P-glycoprotein (P-gp) và có thể ức chế chất vận chuyển này.
Ritonavir có thể gây ra quá trình glucuronid hóa và oxy hóa bởi CYP1A2, CYP2C8, CYP2C9 và CYP2C19, do đó có tác dụng làm tăng chuyển hóa sinh học của một số sản phẩm thuốc được chuyển hóa theo những con đường này và có thể dẫn đến giảm hơn nữa. phơi nhiễm toàn thân với các sản phẩm thuốc đó, có thể làm giảm hoặc rút ngắn tác dụng điều trị của chúng.
Việc sử dụng đồng thời các cơ chất khác của CYP3A4 có thể dẫn đến các tương tác đáng kể tiềm tàng chỉ nên được xem xét nếu lợi ích vượt trội so với rủi ro
Nirmatrelvir/ritonavir là chất nền của CYP3A; do đó, các sản phẩm thuốc cảm ứng CYP3A có thể làm giảm nồng độ nirmatrelvir và ritonavir trong huyết tương và làm giảm tác dụng điều trị của Thuốc Ritonir
Khả năng sinh sản, mang thai và giai đoạn cho con bú
Phụ nữ có khả năng sinh con/Tránh thai ở đối tượng cả nam và nữ
Không có dữ liệu trên người về việc sử dụng Thuốc Ritonir trong thời kỳ mang thai để thông báo về nguy cơ phát triển bất lợi liên quan đến thuốc và phụ nữ trong giai đoạn sinh đẻ nên tránh mang thai trong khi điều trị Thuốc Ritonir
Sử dụng hoạt cháta ritonavir có thể sẽ làm giảm hiệu quả của các biện pháp tránh thai nội tiết tố kết hợp. Bệnh nhân sử dụng thuốc tránh thai nội tiết kết hợp nên được khuyên sử dụng một biện pháp tránh thai khác nhằm thay thế hiệu quả hoặc một biện pháp tránh thai bổ sung trong quá trình điều trị và cho đến sau một chu kỳ kinh nguyệt hoàn chỉnh sau khi ngừng Thuốc Ritonir
Thai kỳ
Không có dữ liệu về việc sử dụng Thuốc Ritonir ở phụ nữ trong thời kì mang thai. Thuốc Ritonir không được khuyến cáo trong thời kỳ mang thai và ở phụ nữ có khả năng sinh con không sử dụng biện pháp tránh thai hiệu quả.
Không có tác dụng liên quan đến nirmatrelvir đối với hình thái của thai nhi hoặc khả năng sống sót của phôi ở bất kỳ liều nào được thử nghiệm trong các nghiên cứu về độc tính phôi ở chuột hoặc thỏ
Một số lượng lớn phụ nữ mang thai đã tiếp xúc với ritonavir trong thời kỳ mang thai.
Những dữ liệu này chủ yếu đề cập đến phơi nhiễm khi ritonavir được sử dụng trong liệu pháp phối hợp và không phải ở liều điều trị của ritonavir mà ở liều điều trị thấp hơn, đóng vai trò như một chất tăng cường dược động học cho các chất ức chế protease khác, tương tự như liều dùng thành phần ritonavir được sử dụng cho nirmatrelvir/ritonavir.
Những dữ liệu được liệt kê này cho thấy tỷ lệ dị tật bẩm sinh không tăng so với tỷ lệ quan sát được trong các hệ thống giám sát dị tật bẩm sinh dựa vào dân số. Dữ liệu trên động vật với ritonavir cho thấy độc tính sinh sản
Cho con bú
Không có dữ liệu của con người về việc sử dụng Thuốc Ritonir trong thời kỳ cho con bú.
Người ta không biết liệu hoạt chất nirmatrelvir có được bài tiết qua sữa người hay động vật hay không và ảnh hưởng của nó đối với trẻ bú mẹ/trẻ sơ sinh hoặc sản xuất sữa. Dữ liệu được công bố hạn chế báo cáo rằng ritonavir có trong sữa mẹ. Không có thông tin về tác dụng của ritonavir đối với trẻ bú mẹ/trẻ sơ sinh hoặc tác dụng của nó đối với việc sản xuất sữa. Không thể loại trừ nguy cơ xấu xảy ra đối với trẻ sơ sinh. Nên ngừng cho con bú trong khi điều trị bằng Thuốc Ritonir và trong 7 ngày sau liều Thuốc Ritonir cuối cùng.
Khả năng sinh sản
Không có dữ liệu của con người về ảnh hưởng của Thuốc Ritonir đối với khả năng sinh sản. Không có dữ liệu của con người về tác dụng của nirmatrelvir đối với khả năng sinh sản. Nirmatrelvir không tạo ra ảnh hưởng đến khả năng sinh sản ở chuột
Không có dữ liệu trên người về ảnh hưởng của ritonavir đối với khả năng sinh sản. Ritonavir không ảnh hưởng đến khả năng sinh sản ở chuột.
Ảnh hưởng đến khả năng lái xe và vận hành máy móc
Không có nghiên cứu lâm sàng nào đánh giá ảnh hưởng của Thuốc Ritonir đối với khả năng lái xe và vận hành máy móc.
Tác dụng không mong muốn khi dùng thuốc Ritonir
Độ an toàn của Thuốc Ritonir dựa trên dữ liệu từ Nghiên cứu C4671005 (EPIC-HR), một thử nghiệm ngẫu nhiên, có đối chứng giả dược Giai đoạn 2/3 ở những người tham gia trưởng thành không nhập viện được chẩn đoán nhiễm trùng SARS-CoV-2 trong phòng thí nghiệm.
Tổng cộng có 1.349 người tham gia là người lớn có triệu chứng từ 18 tuổi trở lên có nguy cơ cao mắc bệnh COVID-19 nghiêm trọng đã nhận ít nhất một liều Thuốc Ritonir(nirmatrelvir/ritonavir 300 mg/100 mg) (n=672 ) hoặc giả dược (n=677) . Thuốc nghiên cứu được dùng hai lần mỗi ngày trong tối đa 5 ngày.
Các phản ứng bất lợi ở nhóm Thuốc Ritonir(≥ 1%) xảy ra với tần suất cao hơn so với nhóm giả dược là tiêu chảy (3,9% và 1,9% tương ứng), nôn (1,3% và 0,3%) và rối loạn vị giác (4,8% và 0,1%).
Một số phản ứng bất lợi:
Rối loạn hệ thần kinh
Rối loạn hệ tiêu hóa
Trẻ em
Tính an toàn và hiệu quả của Thuốc Ritonir ở bệnh nhi chưa được thiết lập.
Quá liều Thuốc
Điều trị cho bệnh nhân dùng quá liều Thuốc Ritonir nên bao gồm các biện pháp giúp hỗ trợ chung bao gồm theo dõi các dấu hiệu và theo dõi tình trạng lâm sàng của bệnh nhân. Không có thuốc giải độc đặc hiệu cho quá liều Thuốc Ritonir.
Đặc tính dược lực học
Cơ chế hoạt động
Thành phần Nirmatrelvir chứa trong thuốc là một chất ức chế peptidomimetic của protease giống coronavirus 3C (3CL), bao gồm cả protease SARS-CoV-2 3CL. Sự ức chế protease 3CL làm cho protein không có khả năng xử lý tiền chất polyprotein dẫn đến ngăn chặn sự nhân lên của virus. Nirmatrelvir đã được chứng minh là chất ức chế mạnh protease SARS-CoV-2 3CL (Ki=0,00311 μM hoặc IC 50 = 0,0192 μM) trong một thử nghiệm enzyme sinh hóa.
Thành phần Ritonavir chứa trong thuốc không hoạt động chống lại protease SARS-CoV-2 3CL. Ritonavir ức chế chuyển hóa qua trung gian CYP3A của nirmatrelvir, do đó làm tăng nồng độ nirmatrelvir trong huyết tương
Hoạt động chống vi-rút
Hoạt tính kháng virus in vitro
Nirmatrelvir thể hiện hoạt tính kháng vi-rút chống lại nhiễm trùng SARS-CoV-2 bởi các tế bào dNHBE, một dòng tế bào biểu mô phế nang phổi nguyên phát của con người (giá trị EC 90 là 181 nM) sau lần lây nhiễm thứ 3.
Hoạt tính kháng vi-rút in vivo
Nirmatrelvir cho thấy hoạt tính kháng vi-rút trong các mô hình chuột nhiễm SAR-CoV-2 thích nghi ở BALB/c và 129 chủng chuột. Sử dụng nirmatrelvir đường uống ở mức 300 mg/kg hoặc 1.000 mg/kg hai lần mỗi ngày bắt đầu 4 giờ sau khi tiêm vắc-xin hoặc 1.000 mg/kg hai lần mỗi ngày bắt đầu 12 giờ sau khi tiêm vắc-xin SARS-CoV-2 MA10 giúp giảm hiệu giá vi-rút phổi và cải thiện các chỉ số bệnh (giảm cân và bệnh lý phổi) so với động vật được điều trị bằng giả dược.
Kháng vi-rút
Vì nirmatrelvir được dùng cùng với ritonavir liều thấp nên có thể có nguy cơ HIV-1 phát triển khả năng kháng thuốc ức chế protease HIV ở những đối tượng bệnh nhân bị nhiễm HIV-1 không được kiểm soát hoặc không được chẩn đoán.
Tác dụng dược lực học
Điện sinh lý tim
Không quan sát thấy tác dụng liên quan về mặt lâm sàng của nirmatrelvir đối với khoảng QTcF trong một nghiên cứu chéo ngẫu nhiên, mù đôi, có đối chứng với giả dược ở 10 người trưởng thành khỏe mạnh. Mô hình dự đoán giới hạn trên của khoảng tin cậy (CI) 90% đối với ước tính QTcF ban đầu và ritonavir đã điều chỉnh là 1,96 ms ở nồng độ cao hơn khoảng 4 lần so với nồng độ đỉnh trung bình ở mức ban đầu. trạng thái ổn định sau liều điều trị của nirmatrelvir/ritonavir 300 mg/100 mg.
Đặc tính dược động học
Cơ chế dược động học của nirmatrelvir/ritonavir đã được nghiên cứu ở những người tham gia khỏe mạnh.
Hoạt chất Ritonavir dùng đồng thời với hoạt chất nirmatrelvir như một chất tăng cường dược động học dẫn đến nồng độ nirmatrelvir toàn thân cao hơn.
Ở những người tham gia khỏe mạnh trong tình trạng đói, thời gian bán thải trung bình (t 1/2) của một liều duy nhất 150 mg nirmatrelvir dùng một mình là khoảng 2 giờ so với 7 giờ sau khi dùng một liều duy nhất. Do đó, 250 mg/100 mg nirmatrelvir/ritonavir hỗ trợ chế độ dùng thuốc hai lần mỗi ngày.
Sau một liều duy nhất nirmatrelvir/ritonavir 250 mg/100 mg cho những người tham gia khỏe mạnh lúc đói, nồng độ tối đa trung bình hình học (CV%) (C max) và diện tích dưới đường cong nồng độ nồng độ trong huyết tương thời gian từ 0 đến lần đo cuối cùng (AUC cuối cùng) là 2,88 ug/mL (25%) và 27,6 ug*giờ/mL (13%).
Với liều lặp lại nirmatrelvir/ritonavir 75 mg/100 mg, 250 mg/100 mg và 500 mg/100 mg hai lần mỗi ngày, sự gia tăng nồng độ toàn thân ở trạng thái ổn định dường như ít hơn tỷ lệ với liều. số lượng. Đa liều trong 10 ngày đạt trạng thái ổn định vào Ngày thứ 2 với sự tích lũy khoảng 2 lần. Phơi nhiễm toàn thân vào Ngày 5 tương tự như Ngày 10 đối với tất cả các liều
Hấp thụ
Sau khi uống nirmatrelvir/ritonavir 300 mg/100 mg với liều duy nhất, giá trị trung bình hình học của nirmatrelvir (CV%) C tối đa và diện tích dưới đường cong nồng độ trong huyết tương theo thời gian từ 0 đến vô cùng ( AUC inf ) ở trạng thái ổn định là 2,21 µg/ mL (33) và 23,01 µg*hr/mL (23), tương ứng. Thời gian trung bình (phạm vi) để C max (T max ) là 3,00 giờ (1,02-6,00). Thời gian bán thải cuối cùng trung bình số học (+SD) là 6,1 (1,8) giờ.
Sau khi uống nirmatrelvir/ritonavir 300 mg/100 mg như một liều duy nhất, giá trị trung bình hình học của ritonavir (CV%) C max và AUC inf lần lượt là 0,36 µg/mL (46) và 3,60. µg*giờ/mL (47). Thời gian trung bình (phạm vi) đến C max (T max ) là 3,98 giờ (1,48-4,20). Thời gian bán thải cuối cùng trung bình số học (+SD) là 6,1 (2,2) giờ.
Ảnh hưởng của thức ăn đến sự hấp thu qua đường miệng
Dùng với bữa ăn nhiều chất béo làm tăng vừa phải nồng độ nirmatrelvir (tăng khoảng 15% C trung bình và tăng 1,6% AUC trung bình ở giai đoạn cuối) so với điều kiện nhịn ăn sau khi dùng nirmatrelvir. Việc đình chỉ sẽ được thực hiện với viên nén ritonavir.
Phân bổ
Sự gắn kết với protein của nirmatrelvir trong huyết tương người là khoảng 69%.
Sự gắn kết với protein của ritonavir trong huyết tương người là khoảng 98-99%.
Biến đổi sinh học
Các nghiên cứu in vitro đánh giá nirmatrelvir không dùng đồng thời với ritonavir đã chỉ ra rằng nirmatrelvir được chuyển hóa chủ yếu bởi CYP3A4. Nirmatrelvir không ức chế thuận nghịch CYP2D6, CYP2C9, CYP2C19, CYP2C8 hoặc CYP1A2 trong ống nghiệm ở các nồng độ phù hợp về mặt lâm sàng. Các nghiên cứu in vitro cho thấy nirmatrelvir có thể cảm ứng CYP3A4, CYP2B6, CYP2C8 và CYP2C9.
Dựa trên dữ liệu in vitro, nirmatrelvir có khả năng ức chế thấp BCRP, MATE2K, OAT1, OAT3, OATP1B3 và OCT2. Nirmatrelvir có khả năng ức chế MDR1, MATE1, OCT1 và OATP1B1 ở nồng độ phù hợp về mặt lâm sàng. Quản lý nirmatrelvir với ritonavir ức chế sự chuyển hóa của nirmatrelvir. Trong huyết tương, thực thể liên quan đến thuốc duy nhất được quan sát thấy là nirmatrelvir không đổi. Các chất chuyển hóa oxy hóa nhỏ được quan sát thấy trong phân và nước tiểu.
Các nghiên cứu in vitro sử dụng microsome gan người đã chứng minh rằng cytochrom P450 3A (CYP3A) là dạng đồng phân chính tham gia vào quá trình chuyển hóa của ritonavir, mặc dù CYP2D6 cũng góp phần hình thành chất chuyển hóa bị oxy hóa M-2. .
Ritonavir liều thấp đã cho thấy tác dụng sâu sắc đối với dược động học của các chất ức chế protease khác (và các sản phẩm khác được chuyển hóa bởi CYP3A4) và các chất ức chế protease khác có thể ảnh hưởng đến dược động học của ritonavir
Hoạt chất Ritonavir có ái lực cao với một số đồng dạng cytochrom P450 (CYP) và có thể ức chế quá trình oxy hóa theo thứ tự xếp hạng sau: CYP3A4 > CYP2D6. Hoạt chất Ritonavir chứa trong thuốc cũng có ái lực cao với P-glycoprotein (P-gp) và có thể ức chế chất vận chuyển này.
Ritonavir có thể gây ra quá trình glucuronid hóa và oxy hóa bởi CYP1A2, CYP2C8, CYP2C9 và CYP2C19, do đó làm tăng chuyển hóa sinh học của một số các loại sản phẩm thuốc được chuyển hóa theo những con đường này và có thể dẫn đến giảm hơn nữa. phơi nhiễm toàn thân với các sản phẩm thuốc đó, có thể làm giảm hoặc rút ngắn tác dụng điều trị của chúng.
Loại bỏ
Con đường thải trừ chính của nirmatrelvir khi dùng đồng thời với ritonavir là bài tiết qua thận dưới dạng thuốc không đổi. Khoảng 49,6% và 35,3% liều nirmatrelvir 300 mg được tìm thấy tương ứng trong nước tiểu và phân. Nirmatrelvir là thực thể chủ yếu liên quan đến thuốc với một lượng nhỏ chất chuyển hóa phát sinh từ các phản ứng thủy phân trong phân. Trong huyết tương, thực thể liên quan đến thuốc có thể định lượng duy nhất là nirmatrelvir không đổi.
Các nghiên cứu trên người với ritonavir được đánh dấu phóng xạ đã chứng minh rằng việc loại bỏ ritonavir chủ yếu thông qua hệ thống gan mật; khoảng 86% chất đánh dấu phóng xạ được thu hồi từ phân, một phần trong số đó được cho là ritonavir không được hấp thu. Ritonavir có ái lực cao với một số dạng đồng phân cytochrom P450 (CYP) và có thể ức chế quá trình này. chất oxy hóa theo thứ tự xếp hạng sau: CYP3A4 > CYP2D6.
Thành phần Ritonavir chứa trong thuốc cũng có ái lực cao với P-glycoprotein (P-gp) và có thể ức chế chất vận chuyển này. Ritonavir có thể gây ra quá trình glucuronid hóa và oxy hóa bởi CYP1A2, CYP2C8, CYP2C9 và CYP2C19, do đó làm tăng chuyển hóa sinh học của một số sản phẩm thuốc được chuyển hóa theo những con đường này và có thể dẫn đến giảm hơn nữa. phơi nhiễm toàn thân với các sản phẩm thuốc đó, có thể làm giảm hoặc rút ngắn tác dụng điều trị của chúng.
Thải trừ
Con đường thải trừ chính của nirmatrelvir khi dùng đồng thời với ritonavir là bài tiết qua thận dưới dạng thuốc không đổi. Khoảng 49,6% và 35,3% liều nirmatrelvir 300 mg được tìm thấy tương ứng trong nước tiểu và phân. Nirmatrelvir là thực thể chủ yếu liên quan đến thuốc với một lượng nhỏ chất chuyển hóa phát sinh từ các phản ứng thủy phân trong phân. Trong huyết tương, thực thể liên quan đến thuốc có thể định lượng duy nhất là nirmatrelvir không đổi.
Các nghiên cứu trên người với ritonavir được đánh dấu phóng xạ đã chứng minh rằng việc loại bỏ ritonavir chủ yếu thông qua hệ thống gan mật; Khoảng 86% chất đánh dấu phóng xạ được thu hồi từ phân, một phần trong số đó được cho là ritonavir không được hấp thu.
Thuốc Ritonir có hiệu quả trong việc chống lại các biến thể mới không?
Thuốc Ritonir hoạt động bằng cách tạo ra các kháng thể giúp tấn công protein đột biến của vi-rút corona – một phần của vi-rút giúp nó xâm nhập vào tế bào người. Các biến thể mới là phản ứng của vi-rút đối với các kháng thể đó, vì vi-rút corona cố gắng thay đổi cách nó bảo vệ chống lại vắc-xin.
Ngược lại, thuốc kháng vi-rút hoạt động bằng cách tấn công các phần khác trong vòng đời của vi-rút corona, làm gián đoạn quá trình vi-rút tự nhân lên. Do đó, các chuyên gia về các bệnh truyền nhiễm tin rằng thuốc này sẽ có hiệu quả chống lại các biến thể mới nhất của COVID-19.
Thuốc Ritonir có tác dụng giống thuốc Paxlovid không?
Thuốc Paxlovid là thuốc biệt dược gốc do công ty Pfizer nghiên cứu và sản xuất có khả năng hoạt động chống lại các biến chủng mới của Virus Covid-19
Thuốc Ritonir là thuốc Generic do công ty Heet – Health Care sản xuất, có thành phần hoạt chất tương tự thuốc biệt dược gốc Paxlovid. Vì vậy, Thuốc Ritonir có công dụng tương tự như thuốc Paxlovid.
Bởi vì, thuốc Generic là bản sao của thuốc biệt dược với thành phần hoạt chất tương tự nhau. Do đó, thuốc biệt dược và thuốc Generic có tên hoạt chất và hiệu quả điều trị tương tự. Như vậy, để có được sự chấp thuận cho đăng ký và bán một loại thuốc, công ty sản xuất cần phải chứng minh rằng thuốc Generic có tác dụng tương tự và đáp ứng các tiêu chuẩn cao tương đương thuốc biệt dược. Như vậy, quá trình phê duyệt thuốc Generic diễn ra rất nghiêm ngặt.
Các thuốc tương tự:
Thuốc Ritonir giá bao nhiêu?
Để mua được sản phẩm thuốc với giá tốt, khuyến cáo khách hàng nên trực tiếp đến mua thuốc tại các bệnh viện tuyến trên hoặc các nhà thuốc có quy mô lớn. Tại đó, bệnh nhân sẽ được mua Thuốc Ritonir với giá thành hợp lý.
Để biết thêm chi thông tin về giá Thuốc Ritonir và các thuốc khác, vui lòng liên hệ số điện thoại hotline của nhathuochapu 0923 283 003 để được tư vấn nhanh chóng. Chúng tôi cam kết bán thuốc Ritonir uy tín với giá tốt nhất.

Thuốc Ritonir mua ở đâu?
Nếu quí khách hàng chưa biết Thuốc Ritonir mua ở đâu tại các địa chỉ ở các nơi khác như Hà Nội, HCM, Đà Nẵng… thì nhathuochapu xin giới thiệu tới quý khách hàng một số địa chỉ để có thể mua được sản phẩm Thuốc Ritonir chất lượng, chính hãng, uy tín, có thể tham khảo, tìm mua như:
*Cơ sở bán thuốc
Cơ sở 1: Trung tâm Phân phối thuốc, số 85 Vũ Trọng Phụng, P.Thanh Xuân Trung, Q.Thanh Xuân, TP. Hà Nội.
Cơ sở 2: Chung Cư Bình Thới, P.8, Q.11, TP. Hồ Chí Minh.
Cơ sở 3: Nguyễn Sinh Sắc, Q. Liên Chiểu, TP. Đà Nẵng.
Facebook: https://www.facebook.com/nhathuochapu
Website: https://nhathuochapu.vn/

Ở các tỉnh thành khác, Chúng tôi có dịch vụ hỗ trợ quý khách mua thuốc Ritonir chính hãng, ship thuốc COD qua các đơn vị vận chuyển uy tín như GHTK, GHN, Viettel Post, VN Post… Quý khách nhận thuốc, kiểm tra rồi mới thanh toán tiền.
Danh sách các Tỉnh, Thành Phố chúng tôi cung cấp thuốc Ritonir: An Giang, Bà Rịa – Vũng Tàu, Bắc Giang, Bắc Kạn, Bạc Liêu, Bắc Ninh, Lâm Đồng, Lạng Sơn, Lào Cai, Long An, Nam Định, Nghệ An, Ninh Bình, Ninh Thuận, Phú Thọ, Quảng Bình, Quảng Nam, Quảng Ngãi, Quảng Ninh, Quảng Trị, Sóc Trăng, Sơn La, Tây Ninh, Thái Bình, Thái Nguyên, Gia Lai, Hà Giang, Hà Nam, Hà Tĩnh, Hải Dương, Hậu Giang, Hòa Bình, Hưng Yên, Khánh Hòa, Kiên Giang, , Thanh Hóa, Thừa Thiên Huế, Tiền Giang, Trà Vinh, Tuyên Quang, Vĩnh Long, Vĩnh Phúc, Yên Bái, Phú Yên, Cần Thơ, Đà Nẵng, Hải Phòng, Hà Nội, TP HCM, Bến Tre, Bình Định, Bình Dương, Bình Phước, Bình Thuận, Cà Mau, Cao Bằng, Đắk Lắk, Đắk Nông, Điện Biên, Đồng Nai, Đồng Tháp, Kon Tum, Lai Châu. Các tỉnh thành này bạn chỉ cần liên hệ số 0923.283.003 để được nhận thuốc tại nhà.
Đối với các quận huyện của Thủ đô Hà Nội và Thành phố Hồ Chí Minh chúng tôi có dịch vụ giao hàng nhanh trong vòng 2 tiếng. Danh sách các Quận huyện mà chúng tôi có dịch vụ cung cấp thuốc Ritonir Quận Ba Đình, Quận Hoàn Kiếm, Quận Hai Bà Trưng, Quận Đống Đa, Quận Tây Hồ, Quận Cầu Giấy, Quận Thanh Xuân, Quận Hoàng Mai, Huyện Hoài Đức, Huyện Thanh Oai, Huyện Mỹ Đức, Huyện Ứng Hòa, Huyện Thường Tín, Huyện Phú Xuyên, Huyện Mê Linh, Quận Nam Từ Liêm, Quận Long Biên, Quận Bắc Từ Liêm, Huyện Thanh Trì, Huyện Gia Lâm, Huyện Đông Anh, Huyện Sóc Sơn, Quận Hà Đông, Thị xã Sơn Tây, Huyện Ba Vì, Huyện Phúc Thọ, Huyện Thạch Thất, Huyện Quốc Oai, Huyện Chương Mỹ, Huyện Đan Phượng: Liên hệ 0923.283.003 để được Ds Đại học Dược Hà Nội tư vấn sử dụng thuốc Ritonir chính hãng, an toàn, hiệu quả.
Nhathuochapu xin chân thành gửi lời cảm ơn tới các quý khách hàng đã quan tâm và dành thời gian tham khảo đọc bài viết về Thuốc Ritonir
Chúc mọi người luôn khỏe mạnh!
Nhathuochapu.vn Chuyên tư vấn, mua bán các loại các loại thuốc kê đơn (Ung thư, viêm gan B, C, thuốc điều trị vô sinh hiếm muộn, kháng sinh…) và các loại thuốc hiếm khó tìm.
Sản phẩm tương tự
Liên hệ để biết giá !
Liên hệ để biết giá !
Liên hệ để biết giá !
Liên hệ để biết giá !